Экспертиза жилого дома – нормативные документы
При диагностическом обследовании и составлении экспертного заключения использовались следующие нормативные документы:
СП 13-102-2003 Правила обследования несущих строительных конструкций зданий и сооружений.
Вид документа: Постановление Госстроя России N 153 от 21.08.2003 г. Своды правил по проектированию и строительству.
Принявший орган: Госстрой России.
Статус: Действующий.
Тип документа: Нормативно-технический документ.
Дата начала действия: 21.08.2003 г.
Опубликован: официальное издание, М. Госстрой России, ГУП ЦПП, 2003 год.
СНиП 3.03.01-87 Несущие и ограждающие конструкции.
Вид документа: Постановление Госстроя СССР N 280 от 04.12.1987 г. Строительные нормы и правила РФ.
Принявший орган: Госстрой СССР.
Статус: Действующий.
Тип документа: Нормативно-технический документ.
Дата начала действия: 01.07.1988 г.
Опубликован: Официальное издание, Минстрой России, — М. ГП ЦПП, 1996 год.
СНиП 2.03.13-88 Полы. Постановление Госстроя СССР от 16.05.1988 N 82
СНиП от 16.05.1988 N 2.03.13-88.Строительные нормы и правила РФ.
Принявший орган: Госстрой СССР.
Статус: Действующий.
Тип документа: Нормативно-технический документ.
Дата начала действия: 01.01.1989
Опубликован: официальное издание, М.: Госстрой России, ГУП ЦПП, 2001 год.
ГОСТ 10950-78 Пиломатериалы и заготовки. Антисептирование способом погружения (с Изменениями N 1-4)
Вид документа:
Постановление Госстандарта СССР от 06. 01.1978 N 25
01.1978 N 25
ГОСТ от 06.01.1978 N 10950-78
Принявший орган: Госстандарт СССР
Статус: Действующий
Тип документа: Нормативно-технический документ
Дата начала действия: 01.01.1979
Опубликован: официальное издание, Пиломатериалы. Общие нормы: Сб. ГОСТов. — М.: ИПК Издательство стандартов, 2002 год
Дата редакции: 01.05.2002
ГОСТ 2140-81 (CT СЭВ 2017-79, СТ СЭВ 2018-79, CT СЭВ 2019-79, СТ СЭВ 320-76, СТ СЭВ 321-76, СТ СЭВ 391-76, СТ СЭВ 3286-81, СТ СЭВ 3287-81, …) Видимые пороки древесины. Классификация, термины и определения, способы измерения (с Изменениями N 1, 2)
Вид документа:
Постановление Госстандарта СССР от 30.06.1981 N 3239
ГОСТ от 30.06.1981 N 2140-81
Принявший орган: Госстандарт СССР
Статус: Действующий
Тип документа: Нормативно-технический документ
Дата начала действия: 01. 01.1982
01.1982
Опубликован: официальное издание, М.: ИПК Издательство стандартов, 1997 год
Дата редакции: 01.05.1997
СП 31-105-2002 группа Ж42 Свод правил по проектированию и строительству. Проектирование и строительство энергоэффективных одноквартирных жилых домов с деревянным каркасом. Design and construction of wood-frame single family houses. ОКС 91.040.30 ОКСТУ 2030
Дата введения 2002-07-01
СНиП 2.02.01-83* Основания зданий и сооружений
Вид документа:
Постановление Госстроя СССР от 05.12.1983 N 311 СНиП от 05.12.1983 N 2.02.01-83*
Принявший орган: Госстрой СССР
Статус: Действующий
Тип документа: Нормативно-технический документ
Дата начала действия: 01.01.1985
Опубликован: официальное издание, / Минстрой России. — М.: ГП ЦПП, 1995 год
— М.: ГП ЦПП, 1995 год
Дата редакции: 09.12.1985
ГОСТ 8486-86 (СТ СЭВ 2369-80) Пиломатериалы хвойных пород. Технические условия (с Изменениями N 1, 2, 3)
Вид документа:
Постановление Госстандарта СССР от 30.09.1986 N 2933
ГОСТ от 30.09.1986 N 8486-86
Принявший орган: Госстандарт СССР
Статус: Действующий
Тип документа: Нормативно-технический документ
Дата начала действия: 01.01.1988
Опубликован: официальное издание, Пиломатериалы, заготовки, деревянные детали:
Сб. ГОСТов. — М.: Издательство стандартов, 1990 год
Дата редакции: 01.05.1990
СНиП 3.04.01-87 «Изоляционные и отделочные покрытия»
Вид документа: Постановление Госстроя СССР от 04.12.1987 N 280
СНиП от 04.12.1987 N 3.04.01-87
Принявший орган: Госстрой СССР
Статус: Действующий
Тип документа: Нормативно-технический документ
Дата начала действия: 01. 07.1988
07.1988
Опубликован: официальное издание, Госстрой России. — М.: ГУП ЦПП, 1998 год
ВСН 57-88(р) «Положение по техническому обследованию жилых зданий»
Вид документа: Приказ Госстроя СССР от 06.07.1988 N 191
ВСН от 06.07.1988 N 57-88(Р) Своды правил по проектированию и строительству
Принявший орган: Госстрой СССР
Статус: Действующий
Тип документа: Нормативно-технический документ
Дата начала действия: 01.07.1989
Опубликован: официальное издание, Госкомархитектура — М.: 1991 год
МДС 12-33.2007 Кровельные работы
Вид документа:
МДС от 01.01.2007 N 12-33.2007
Инструктивно-методические документы
Принявший орган: Различные информационные источники
Статус: Действующий
Тип документа: Нормативно-технический документ
Классификатор основных видов дефектов в строительстве и промышленности строительных материалов
Вид документа: Приказ Главгосархстройнадзора России от 17. 11.1993
11.1993
Нормы, правила и нормативы органов государственного надзора
Принявший орган: Главгосархстройнадзор России
Статус: Действующий
Тип документа: Нормативно-технический документ
Опубликован: Официальное издание
СП 50-101-2004 Проектирование и устройство оснований и фундаментов зданий и сооружений
Вид документа: Постановление Госстроя России от 09.03.2004 N 28
Свод правил (СП) от 09.03.2004 N 50-101-2004
Своды правил по проектированию и строительству
Принявший орган: Госстрой России
Статус: Действующий
Тип документа: Нормативно-технический документ
Опубликован: официальное издание, М.: ФГУП ЦПП, 2005 год
ГОСТ 9330-76 Основные соединения деталей из древесины и древесных материалов. Типы и размеры (с Изменениями N 1, 2)
Вид документа: Постановление Госстандарта СССР от 11. 05.1976 N 1161
05.1976 N 1161
ГОСТ от 11.05.1976 N 9330-76
Принявший орган: Госстандарт СССР
Статус: Действующий
Тип документа: Нормативно-технический документ
Дата начала действия: 01.07.1977
Опубликован: официальное издание, Пиломатериалы. Общие нормы: Сб. ГОСТов. — М.: ИПК Издательство стандартов, 2002 год
Дата редакции: 01.05.2002
СНиП 3.04.01-87 «Изоляционные и отделочные покрытия»
Вид документа: Постановление Госстроя СССР от 04.12.1987 N 280
СНиП от 04.12.1987 N 3.04.01-87
Принявший орган: Госстрой СССР
Статус: Действующий
Тип документа: Нормативно-технический документ
Дата начала действия: 01.07.1988
Опубликован: официальное издание, Госстрой России. — М.: ГУП ЦПП, 1998 год
Приведенные и использованные при составлении заключения правовые и нормативно-технические ссылки даны на основании действующих документов приведенных в специализированной справочной системе «Стройэксперт-кодекс».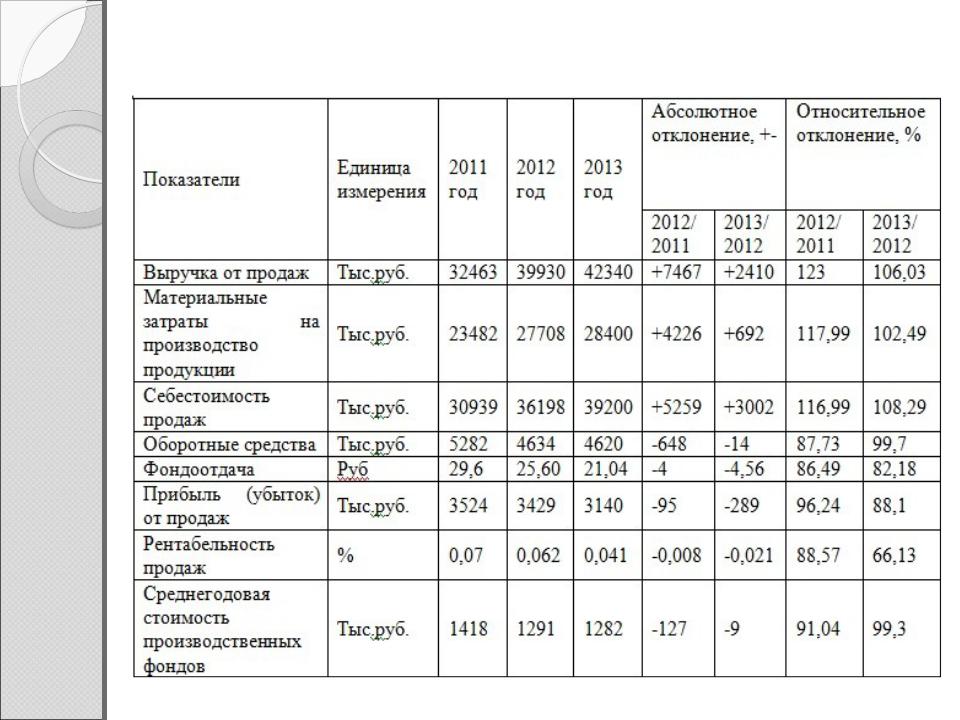
Лицензия на ПК КОДЕКС для Windows (сетевой вариант) зарегистрирована в ЗАО “Независимое агентство строительных экспертиз”.
СП 53.13330.2019 «Планировка и застройка территории ведения гражданами садоводства. Здания и сооружения» (СНиП 30-02-97* Планировка и застройка территорий садоводческих (дачных) объединений граждан, здания и сооружения)
Опубликовано: 14 октября 2019
Реквизиты для осуществления перевода денежных средств в доход федерального бюджетаРекомендации в целях определения оптимальных процедур взаимодействия уполномоченных банков и застройщиков при переходе на проектное финансирование объектов долевого жилищного строительства с использованием счетов эскроу для учета и использования в работе застройщиками, реализующими проекты долевого жилищного строительства с использованием счетов эскроу, финансируемые за счет кредитов, и соответствующими кредитными организациями, осуществляющими кредитование указанных застройщиковПосмотреть СкачатьОб обязанности застройщиков по уплате обязательных отчислений (взносов) в компенсационный фондПриказ Минстроя России от 27. 09.2015 г. № 771/пр “Об утверждении Административного регламента по исполнению Министерством строительства и жилищно-коммунального хозяйства Российской Федерации государственной функции по осуществлению государственного контроля (надзора) за деятельностью саморегулируемых организаций в сфере теплоснабжения”
09.2015 г. № 771/пр “Об утверждении Административного регламента по исполнению Министерством строительства и жилищно-коммунального хозяйства Российской Федерации государственной функции по осуществлению государственного контроля (надзора) за деятельностью саморегулируемых организаций в сфере теплоснабжения” №819 “О Министерстве строительства и жилищно-коммунального хозяйства Российской Федерации”Посмотреть
Скачать Приказ Министерства строительства и жилищно-коммунального хозяйства Российской Федерации (Минстрой России) от 5 мая 2014 г. № 223/пр г. Москва “Об утверждении условий отнесения жилых помещений к жилью экономического класса”Посмотреть
СкачатьПриказ Минстроя России от 18 июня 2014 года № 321/пр О внесении изменений в перечень субъектов Российской Федерации, на территории которых осуществляется реализация программы «Жилье для российской семьи» в рамках государственной программы РФ «Обеспечение доступным и комфортным жильем и коммунальными услугами граждан Российской Федерации», утвержденный приказом Министерства строительства и жилищно-коммунального хозяйства от 27 мая 2014 года №258/пр.Посмотреть
СкачатьФедеральный закон от 21 июля 2014 года № 217-ФЗ “О внесении изменений в Жилищный кодекс Российской Федерации и отдельные законодательные акты Российской Федерации в части законодательного регулирования отношений по найму жилых помещений жилищного фонда социального использования”
№819 “О Министерстве строительства и жилищно-коммунального хозяйства Российской Федерации”Посмотреть
Скачать Приказ Министерства строительства и жилищно-коммунального хозяйства Российской Федерации (Минстрой России) от 5 мая 2014 г. № 223/пр г. Москва “Об утверждении условий отнесения жилых помещений к жилью экономического класса”Посмотреть
СкачатьПриказ Минстроя России от 18 июня 2014 года № 321/пр О внесении изменений в перечень субъектов Российской Федерации, на территории которых осуществляется реализация программы «Жилье для российской семьи» в рамках государственной программы РФ «Обеспечение доступным и комфортным жильем и коммунальными услугами граждан Российской Федерации», утвержденный приказом Министерства строительства и жилищно-коммунального хозяйства от 27 мая 2014 года №258/пр.Посмотреть
СкачатьФедеральный закон от 21 июля 2014 года № 217-ФЗ “О внесении изменений в Жилищный кодекс Российской Федерации и отдельные законодательные акты Российской Федерации в части законодательного регулирования отношений по найму жилых помещений жилищного фонда социального использования”{{ item. text }}
text }}
{{ item.text }}
{{ inputError }}
Холдинговая компания Scilex, дочерняя компания Sorrento Therapeutics, Inc. с контрольным пакетом акций, объявляет окончательные результаты эффективности и безопасности SP-102 (SEMDEXA™) в рамках основной программы клинических испытаний фазы 3 для лечения боли при ишиасе
- SP-102 (SEMDEXA™), с 401 пациентом, зарегистрированным в C.L.E. .А.Р. (Кортикостероидная пояснично-крестцовая эпидуральная анальгезия при радикулопатии) наблюдалось быстрое начало облегчения боли, измеренное по числовой шкале оценки боли по средней ежедневной боли в пораженной ноге, с высокостатистически значимым улучшением по сравнению с плацебо в течение первых 4 недель после однократной трансфораминальной инъекции.
- SP-102 (SEMDEXA™) продемонстрировал постоянное уменьшение боли в течение одного месяца, а среднее время повторной открытой инъекции составило 99 дней (95% ДИ: 78, 129 дней) в соответствии с оценкой Каплана-Мейера.
 Напротив, инъекционные стероиды, не зарегистрированные по прямому назначению, обычно обеспечивают облегчение боли на период от менее недели до одного месяца, после чего может потребоваться повторная инъекция.
Напротив, инъекционные стероиды, не зарегистрированные по прямому назначению, обычно обеспечивают облегчение боли на период от менее недели до одного месяца, после чего может потребоваться повторная инъекция. - Ключевая вторичная конечная точка индекса инвалидности Освестри, золотого стандарта для измерения степени инвалидности и оценки качества жизни, показала улучшение на 28% через 4 недели на SP-102 (SEMDEXA™) по сравнению с исходным уровнем (минимальное клинически значимое улучшение 8–12%) 15 . Разница среднего значения LS (SEM) по сравнению с плацебо составила -6,28 (1,49) с p-значением <0,001. Анализ безопасности
- показал очень чистый профиль безопасности без выявленных рисков безопасности. Серьезных нежелательных явлений, связанных с препаратом или процедурой инъекции, не было, а также не сообщалось о нежелательных явлениях, представляющих особый интерес, таких как гематома и инфекция в месте инъекции или параплегия. Эти события связаны с использованием вне зарегистрированных показаний неутвержденных инъекционных стероидных препаратов.

ПАЛО-АЛЬТО, Калифорния, 18 марта 2022 г. (GLOBE NEWSWIRE) — Холдинговая компания Scilex («Scilex»), дочерняя компания Sorrento Therapeutics, Inc. (Nasdaq: SRNE, «Sorrento»), сегодня объявила о весьма значимых положительных окончательных результатах своего базового исследования фазы 3 SP-102 (SEMDEXA™) C.L.E. .А.Р. Программа. SP-102 (SEMDEXA™) получил статус Fast Track от FDA.
C.L.E.A.R. Испытание (кортикостероидная пояснично-крестцовая эпидуральная анальгезия при радикулопатии) было разработано для изучения безопасности и обезболивающего действия однократной и повторной трансфораминальной инъекции SP-102 (SEMDEXA™) по сравнению с плацебо (инъекция физиологического раствора). В исследование был включен 401 субъект с болью в пояснице с односторонней грыжей межпозвонкового диска в поясничном отделе позвоночника, что приводило к симптомам корешковой боли от умеренной до сильной боли в ногах. Это крупнейшее известное рандомизированное хорошо контролируемое исследование ишиаса с использованием эпидуральных инъекций стероидов. Первичная конечная точка изменения средней ежедневной боли в пораженной ноге в течение 4 недель после первоначальной инъекции продемонстрировала разницу между средним значением LS (SEM) в группе -1,08 (0,17) по сравнению с плацебо со значением p <0,001. SP-102 (SEMDEXA™) является первым неопиоидным новым инъекционным кортикостероидным гелем, разрабатываемым для лечения поясничной корешковой боли, и он не содержит консервантов, поверхностно-активных веществ, растворителей или твердых частиц.
В исследование был включен 401 субъект с болью в пояснице с односторонней грыжей межпозвонкового диска в поясничном отделе позвоночника, что приводило к симптомам корешковой боли от умеренной до сильной боли в ногах. Это крупнейшее известное рандомизированное хорошо контролируемое исследование ишиаса с использованием эпидуральных инъекций стероидов. Первичная конечная точка изменения средней ежедневной боли в пораженной ноге в течение 4 недель после первоначальной инъекции продемонстрировала разницу между средним значением LS (SEM) в группе -1,08 (0,17) по сравнению с плацебо со значением p <0,001. SP-102 (SEMDEXA™) является первым неопиоидным новым инъекционным кортикостероидным гелем, разрабатываемым для лечения поясничной корешковой боли, и он не содержит консервантов, поверхностно-активных веществ, растворителей или твердых частиц.
Ключевая вторичная конечная точка индекса инвалидности Освестри, золотого стандарта для измерения степени инвалидности и оценки качества жизни, показала улучшение на 28% через 4 недели на SEMDEXA™ по сравнению с исходным уровнем (минимальное клинически значимое улучшение 8–12%) 15 . Разница среднего значения LS (наименьший квадрат) (стандартная ошибка среднего) по сравнению с плацебо составила -6,28 (1,49) с p-значением <0,001.
Разница среднего значения LS (наименьший квадрат) (стандартная ошибка среднего) по сравнению с плацебо составила -6,28 (1,49) с p-значением <0,001.
SP-102 (SEMDEXA™) продемонстрировал облегчение боли, которое продолжалось в течение 12 недель. Другие измерения боли, такие как сильная ежедневная и текущая боль в пораженной ноге и средняя ежедневная боль в нижней части спины, продемонстрировали статистически значимые результаты по сравнению с плацебо. Большинство других вторичных конечных точек в иерархическом расположении для процедуры последовательного тестирования также продемонстрировали статистически значимые результаты и включали общее впечатление об изменении, краткую инвентаризацию боли, PainDETECT и кумулятивное использование спасательных препаратов (ацетаминофен).
Анализ безопасности показал очень чистый профиль безопасности без выявленных рисков безопасности. Серьезных нежелательных явлений, связанных с препаратом или процедурой инъекции, не было, а также не сообщалось о нежелательных явлениях, представляющих особый интерес, таких как гематома и инфекция в месте инъекции или параплегия.
«Мы очень довольны положительным результатом, и эти результаты испытаний очень примечательны. Они окажут большое влияние на сообщество специалистов по лечению боли и позволят нам продолжить реализацию наших планов по регистрации SP-102 (SEMDEXA™) в FDA для лечения подострой пояснично-крестцовой корешковой боли. Мы считаем, что SP-102 (SEMDEXA™) потенциально может стать революционным вариантом лечения ишиаса, области, в которой не наблюдалось значительного прогресса в терапии, которую пациенты и врачи искали на протяжении десятилетий. Мы планируем представить результаты исследования C.L.E.A.R фазы 3 на предстоящих научных конференциях и представить для публикации в рецензируемом журнале», — сказал Дмитрий Лиссин, доктор медицинских наук, главный медицинский директор Scilex.
Мы планируем представить результаты исследования C.L.E.A.R фазы 3 на предстоящих научных конференциях и представить для публикации в рецензируемом журнале», — сказал Дмитрий Лиссин, доктор медицинских наук, главный медицинский директор Scilex.
Scilex намерена использовать результаты этого ключевого исследования фазы 3, чтобы обсудить с FDA в 2022 году требования к заявке на получение лицензии и статус прорыва для показаний с высокой неудовлетворенной потребностью в ишиасе, для которых не было одобрено лечение в США. ), который был разработан для обеспечения длительного местного эффекта и неопиоидного обезболивания у пациентов с ишиасом. Scilex рассчитывает представить надежные данные, собранные в ходе многолетней программы клинических исследований компании, в FDA в рамках заявки на новое лекарство (NDA).
Более 60% назначений опиоидов в США предназначены для лечения хронической боли в пояснице (ХБП) 1 , несмотря на то, что опиоиды связаны с серьезными и потенциально опасными для жизни побочными эффектами и не продемонстрировали свою эффективность при лечении ХБП. 2 , 3 , 4 70%) были связаны с опиоидами. Более 70% из 70 630 смертей в 2019 г.участвовал опиоид. 6 Предварительные данные, опубликованные Центрами по контролю и профилактике заболеваний, показали, что смертность от передозировки наркотиков выросла почти на 29% за 12-месячный период, закончившийся в апреле 2021 года, до примерно 100 306 человек. 7
2 , 3 , 4 70%) были связаны с опиоидами. Более 70% из 70 630 смертей в 2019 г.участвовал опиоид. 6 Предварительные данные, опубликованные Центрами по контролю и профилактике заболеваний, показали, что смертность от передозировки наркотиков выросла почти на 29% за 12-месячный период, закончившийся в апреле 2021 года, до примерно 100 306 человек. 7
«Мы очень рады этим весьма значимым положительным клиническим результатам основного исследования фазы 3 SP-102 (SEMDEXA™), и это может стать обнадеживающей новостью для многих миллионов людей во всем мире, которые сталкиваются с мучительной корешковой болью (ишиасом). Мы считаем, что SP-102 (SEMDEXA™) может стать первым продуктом для эпидуральных инъекций стероидного геля, одобренным FDA, для пациентов, страдающих этим распространенным, очень болезненным состоянием. Я очень ценю работу команды Scilex и их стремление справиться с опиоидным кризисом в Америке и продолжить нашу миссию по улучшению нашей способности помогать миллионам пациентов, страдающих острой и хронической болью, новыми захватывающими способами. Эти окончательные результаты данных знаменуют захватывающую и важную веху на нашем пути к тому, чтобы стать ведущей компанией по лечению боли без опиоидов», — сказал Джайсим Шах, президент и главный исполнительный директор Scilex.
Эти окончательные результаты данных знаменуют захватывающую и важную веху на нашем пути к тому, чтобы стать ведущей компанией по лечению боли без опиоидов», — сказал Джайсим Шах, президент и главный исполнительный директор Scilex.
SP-102 (SEMDEXA™) является первым неопиоидным новым инъекционным кортикостероидным гелем, разрабатываемым для лечения поясничной корешковой боли, и он не содержит консервантов, поверхностно-активных веществ, растворителей или твердых частиц. В случае одобрения FDA препарат SP-102 (SEMDEXA™) будет доступен в форме предварительно заполненного шприца и будет вводиться в виде эпидуральной инъекции для лечения ишиаса. Основываясь на доклинических и клинических исследованиях, SP-102 (SEMDEXA™) продлевает время пребывания в месте инъекции и не вызывает проблем с безопасностью, которые заставили FDA предостеречь от использования других инъекционных стероидных форм эпидуральным путем введения.
В то время как стероиды, используемые не по прямому назначению, обеспечивают облегчение боли на период от менее недели до одного месяца, после чего может потребоваться повторная инъекция, SP-102 (SEMDEXA™) продемонстрировал постоянное уменьшение боли в течение более одного месяца, а среднее время повторной инъекции в открытом режиме составило 99 дней (95% ДИ: 78, 129 дней) согласно оценке Каплана-Мейера.
К 2022 году общее предполагаемое количество процедур эпидуральной инъекции стероидов (ESI) в США, как ожидается, составит 12,1 миллиона для всех пациентов Medicare и частных страховых компаний, при этом процедуры поясничной радикулопатии/ишиаса составляют примерно 88% всех процедур ESI, вводимых согласно собственному исследованию Syneos Health Consulting. Несмотря на широкое использование ESI, на рынке сохраняются опасения по поводу стероидов в виде частиц и потенциальных побочных эффектов и проблем с безопасностью (например, инсульт) от текущего использования не по прямому назначению. В результате на рынке существует значительная неудовлетворенная медицинская потребность в новом препарате ESI, не содержащем частиц, который демонстрирует безопасность и эффективность в контролируемых клинических испытаниях. 14
В США более 30 миллионов человек страдают от поясничной и корешковой боли. Ожидается, что это население будет расти по мере старения населения в целом. 8,9 Многие пациенты испытывают умеренную или сильную боль при непереносимости и/или неадекватном ответе на современные анальгетики, такие как опиоиды и нестероидные противовоспалительные препараты (НПВП). 10,11 Существует большая потребность в высокоэффективных обезболивающих препаратах для облегчения состояния пациентов без проблем с токсичностью и переносимостью НПВП и опиоидов. 9
8,9 Многие пациенты испытывают умеренную или сильную боль при непереносимости и/или неадекватном ответе на современные анальгетики, такие как опиоиды и нестероидные противовоспалительные препараты (НПВП). 10,11 Существует большая потребность в высокоэффективных обезболивающих препаратах для облегчения состояния пациентов без проблем с токсичностью и переносимостью НПВП и опиоидов. 9
Scilex Holding Company и Vickers Vantage Corp. I (Nasdaq: VCKA) («VCKA»), специализированная компания по приобретению, спонсируемая Vickers Venture Fund VI Pte Ltd и Vickers Venture Fund VI (Plan) Pte Ltd, заключили окончательное соглашение об объединении бизнеса («BCA»). После закрытия сделки объединенная компания («Объединенная компания») будет переименована в Scilex Holding Company, и ожидается, что ее обыкновенные акции будут котироваться на Nasdaq под тикером «SCLX». Советы директоров VCKA, Scilex и Sorrento единогласно одобрили предложенную сделку. Закрытие сделки, которое, как ожидается, произойдет к третьему кварталу 2022 года, зависит от одобрения акционеров VCKA и выполнения или отказа от некоторых других обычных условий закрытия.
Закрытие сделки, которое, как ожидается, произойдет к третьему кварталу 2022 года, зависит от одобрения акционеров VCKA и выполнения или отказа от некоторых других обычных условий закрытия.
Корпоративную презентацию, описывающую планы развития Scilex, можно найти на сайте www.scilexholding.com.
О холдинговой компании Scilex
Холдинговая компания Scilex, дочерняя компания Sorrento Therapeutics, Inc. с контрольным пакетом акций, занимается разработкой и коммерциализацией неопиоидных обезболивающих препаратов для лечения острой и хронической боли. Scilex не идет на компромиссы в своем стремлении стать мировым лидером в области лечения боли, приверженным социальным, экологическим, экономическим и этическим принципам ответственной разработки фармацевтических продуктов для максимального качества жизни. Scilex нацелен на показания с высокими неудовлетворенными потребностями и большими рыночными возможностями неопиоидной терапии для лечения пациентов с умеренной и сильной болью. Scilex запустила свой первый коммерческий продукт в октябре 2018 года и разрабатывает свою последнюю стадию конвейера, которая включает в себя ключевого кандидата Фазы 3, а также одного кандидата Фазы 2 и одного кандидата Фазы 1. Его коммерческий продукт, ZTlido® (система для местного применения с лидокаином) 1,8%, или ZTlido®, представляет собой рецептурный препарат с лидокаином для местного применения, одобренный Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для облегчения боли, связанной с постгерпетической невралгией, которая является формой пост-опоясывающего нерва. Три продукта-кандидата Scilex: SP-102 (инъекционный вязкий гель на основе дексаметазона натрия фосфата, содержащий 10 мг дексаметазона) или SEMDEXA™, новый вязкий гель фазы 3, широко используемый кортикостероид для эпидуральных инъекций для лечения пояснично-крестцовой корешковой боли или ишиаса, со статусом FDA Fast Track; SP-103 (система для местного применения с лидокаином) 5,4%, или SP-103, препарат ZTlido® тройной концентрации нового поколения фазы 2 для лечения болей в пояснице; и SP-104, 4,5 мг капсул с отсроченным высвобождением низкой дозы налтрексона гидрохлорида (DBR-LDN) для лечения хронической боли, фибромиалгии в нескольких программах Фазы 1, которые будут начаты в этом году.
Scilex запустила свой первый коммерческий продукт в октябре 2018 года и разрабатывает свою последнюю стадию конвейера, которая включает в себя ключевого кандидата Фазы 3, а также одного кандидата Фазы 2 и одного кандидата Фазы 1. Его коммерческий продукт, ZTlido® (система для местного применения с лидокаином) 1,8%, или ZTlido®, представляет собой рецептурный препарат с лидокаином для местного применения, одобренный Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для облегчения боли, связанной с постгерпетической невралгией, которая является формой пост-опоясывающего нерва. Три продукта-кандидата Scilex: SP-102 (инъекционный вязкий гель на основе дексаметазона натрия фосфата, содержащий 10 мг дексаметазона) или SEMDEXA™, новый вязкий гель фазы 3, широко используемый кортикостероид для эпидуральных инъекций для лечения пояснично-крестцовой корешковой боли или ишиаса, со статусом FDA Fast Track; SP-103 (система для местного применения с лидокаином) 5,4%, или SP-103, препарат ZTlido® тройной концентрации нового поколения фазы 2 для лечения болей в пояснице; и SP-104, 4,5 мг капсул с отсроченным высвобождением низкой дозы налтрексона гидрохлорида (DBR-LDN) для лечения хронической боли, фибромиалгии в нескольких программах Фазы 1, которые будут начаты в этом году. Для получения дополнительной информации об исследовании эффективности фазы 3 SP-102 см. идентификатор NCT NCT03372161 — Кортикостероидная поясничная эпидуральная анальгезия при радикулопатии — Полнотекстовое представление — ClinicalTrials.gov.
Для получения дополнительной информации об исследовании эффективности фазы 3 SP-102 см. идентификатор NCT NCT03372161 — Кортикостероидная поясничная эпидуральная анальгезия при радикулопатии — Полнотекстовое представление — ClinicalTrials.gov.
Холдинговая компания Scilex со штаб-квартирой в Пало-Альто, Калифорния, с операциями как в Пало-Альто, так и в Сан-Диего, Калифорния. Для получения дополнительной информации посетите сайт www.scilexholding.com.
О компании Sorrento Therapeutics, Inc.
Sorrento — это биофармацевтическая компания клинической и коммерческой стадии, разрабатывающая новые методы лечения рака, боли (неопиоидные методы лечения), аутоиммунных заболеваний и COVID-19. Мультимодальный, многоаспектный подход Sorrento к борьбе с раком стал возможен благодаря его обширным иммуноонкологическим платформам, включая ключевые активы, такие как полностью человеческие антитела («библиотека G-MAB™»), иммуноклеточная терапия («DAR-T™»), конъюгаты антитело-лекарственное средство («ADC») и онколитический вирус («Seprehvec™»). Sorrento также разрабатывает потенциальные противовирусные препараты и вакцины против коронавирусов, включая абивертиниб, COVI-AMG™, COVISHIELD™, COVI-MSC™ и COVIDROPS™; и решения для диагностических тестов, включая COVITRACK™ и COVISTIX™.
Sorrento также разрабатывает потенциальные противовирусные препараты и вакцины против коронавирусов, включая абивертиниб, COVI-AMG™, COVISHIELD™, COVI-MSC™ и COVIDROPS™; и решения для диагностических тестов, включая COVITRACK™ и COVISTIX™.
Приверженность компании Sorrento к улучшению жизни пациентов также подтверждается нашими усилиями по продвижению первой в своем классе (агонист TRPV1) неопиоидной малой молекулы для обезболивания, резинифератоксина («RTX») и SP-102 (10 мг, вязкий гель дексаметазона натрия фосфата) (SEMDEXA™), новой вязкой гелевой формы широко используемого кортикостероид для эпидуральных инъекций для лечения пояснично-крестцовой корешковой боли или ишиаса, а также для коммерциализации ZTlido® (лидокаиновая местная система) 1,8% для лечения постгерпетической невралгии (ПГН). RTX был допущен к испытаниям фазы II для лечения непреодолимой боли, связанной с раком, и к испытаниям фазы II у пациентов с остеоартритом. Компания SEMDEXA объявила о высокостатистически значимых положительных результатах своей программы III фазы Pivotal Trial C. L.E.A.R для своего нового неопиоидного продукта для лечения пояснично-крестцовой корешковой боли (ишиаса). ZTlido® был одобрен FDA 28 февраля 2018 г.
L.E.A.R для своего нового неопиоидного продукта для лечения пояснично-крестцовой корешковой боли (ишиаса). ZTlido® был одобрен FDA 28 февраля 2018 г.
Для получения дополнительной информации посетите сайт www.sorrentotherapys.com.
О Vickers Vantage Corp. I
Vickers Vantage Corp. I является компанией-бланшетом, созданной с целью осуществления слияния, обмена акциями, приобретения активов, покупки акций, реорганизации или аналогичного объединения бизнеса с одним или несколькими предприятиями или организациями.
Важная информация и где ее найти
В этом пресс-релизе упоминается предполагаемая сделка между Scilex и VCKA. Настоящий пресс-релиз не является предложением о продаже или обмене или предложением о предложении о покупке или обмене каких-либо ценных бумаг, а также не может осуществляться продажа ценных бумаг в какой-либо юрисдикции, в которой такое предложение, продажа или обмен были бы незаконными до регистрации или квалификации в соответствии с законодательством о ценных бумагах любой такой юрисдикции. В связи с описываемой здесь сделкой VCKA намерена подать соответствующие материалы в SEC, в том числе заявление о регистрации по форме S-4, которое будет включать документ, служащий проспектом эмиссии, и заявление о доверенности VCKA, именуемое заявлением о доверенности/проспектом. После того, как заявление о регистрации будет объявлено SEC вступившим в силу, заявление о доверенности/проспект эмиссии будет разослано всем акционерам VCKA на дату регистрации собрания акционеров VCKA, которое будет назначено для голосования по предлагаемому объединению бизнеса. VCKA также подаст в SEC другие документы, касающиеся предполагаемой сделки. Этот пресс-релиз не содержит всей информации, которая будет содержаться в заявлении о доверенности/проспекте эмиссии или других документах, поданных или подлежащих регистрации в SEC. Прежде чем принимать какое-либо решение о голосовании, инвесторам и держателям ценных бумаг VCKA настоятельно рекомендуется прочитать заявление о регистрации, заявление о доверенности/проспект и все другие соответствующие документы, поданные или которые будут поданы в SEC в связи с предлагаемой сделкой по мере их поступления, поскольку они будут содержать важную информацию о предлагаемой сделке.
В связи с описываемой здесь сделкой VCKA намерена подать соответствующие материалы в SEC, в том числе заявление о регистрации по форме S-4, которое будет включать документ, служащий проспектом эмиссии, и заявление о доверенности VCKA, именуемое заявлением о доверенности/проспектом. После того, как заявление о регистрации будет объявлено SEC вступившим в силу, заявление о доверенности/проспект эмиссии будет разослано всем акционерам VCKA на дату регистрации собрания акционеров VCKA, которое будет назначено для голосования по предлагаемому объединению бизнеса. VCKA также подаст в SEC другие документы, касающиеся предполагаемой сделки. Этот пресс-релиз не содержит всей информации, которая будет содержаться в заявлении о доверенности/проспекте эмиссии или других документах, поданных или подлежащих регистрации в SEC. Прежде чем принимать какое-либо решение о голосовании, инвесторам и держателям ценных бумаг VCKA настоятельно рекомендуется прочитать заявление о регистрации, заявление о доверенности/проспект и все другие соответствующие документы, поданные или которые будут поданы в SEC в связи с предлагаемой сделкой по мере их поступления, поскольку они будут содержать важную информацию о предлагаемой сделке. Инвесторам и держателям ценных бумаг VCKA настоятельно рекомендуется ознакомиться с этими материалами (включая любые поправки или дополнения к ним) и любыми другими соответствующими документами в связи со сделкой, которые VCKA подает в SEC, когда и если они станут доступны, поскольку они будут содержать важную информацию о VCKA, Scilex и предлагаемой сделке. Инвесторы и держатели ценных бумаг смогут получить бесплатные копии заявления о регистрации, заявления о доверенности/проспекта эмиссии и всех других соответствующих документов, поданных или которые будут поданы в SEC VCKA, через веб-сайт, поддерживаемый SEC, по адресу www.sec.gov.
Инвесторам и держателям ценных бумаг VCKA настоятельно рекомендуется ознакомиться с этими материалами (включая любые поправки или дополнения к ним) и любыми другими соответствующими документами в связи со сделкой, которые VCKA подает в SEC, когда и если они станут доступны, поскольку они будут содержать важную информацию о VCKA, Scilex и предлагаемой сделке. Инвесторы и держатели ценных бумаг смогут получить бесплатные копии заявления о регистрации, заявления о доверенности/проспекта эмиссии и всех других соответствующих документов, поданных или которые будут поданы в SEC VCKA, через веб-сайт, поддерживаемый SEC, по адресу www.sec.gov.
Участники ходатайства
VCKA и ее директора и должностные лица могут считаться участниками запроса доверенностей от акционеров VCKA в связи со сделкой. Список имен таких директоров и исполнительных должностных лиц, а также информация об их интересах в предлагаемом объединении бизнеса будет содержаться в заявлении о доверенности/проспекте эмиссии, если таковые имеются. Вы можете получить бесплатные копии этих документов, как описано в предыдущем абзаце.
Вы можете получить бесплатные копии этих документов, как описано в предыдущем абзаце.
Scilex, ее директора и исполнительные директора также могут считаться участниками запроса доверенностей от акционеров VCKA в связи с предлагаемой сделкой. Информация о директорах и исполнительных директорах Scilex, а также информация об их интересах в предлагаемой сделке будет включена в заявление о доверенности/проспект предполагаемой сделки.
Отсутствие предложения
Этот пресс-релиз не является доверенностью или запросом доверенности, согласия или разрешения в отношении каких-либо ценных бумаг или в отношении потенциальной сделки и не должен представлять собой предложение продать или предложение купить ценные бумаги VCKA, Объединенной компании или Scilex, а также не должно быть никаких продаж каких-либо таких ценных бумаг в любом штате или юрисдикции в что такое предложение, ходатайство или продажа были бы незаконными до регистрации или квалификации в соответствии с законами о ценных бумагах такого штата или юрисдикции. Никакое предложение ценных бумаг не может быть сделано, кроме как посредством проспекта, отвечающего требованиям Закона о ценных бумагах от 1933 с поправками.
Никакое предложение ценных бумаг не может быть сделано, кроме как посредством проспекта, отвечающего требованиям Закона о ценных бумагах от 1933 с поправками.
Заявления прогнозного характера
Настоящий пресс-релиз и любые заявления, сделанные во время любой презентации или встречи по вопросам, обсуждаемым в данном пресс-релизе, содержат прогнозные заявления, касающиеся VCKA, Sorrento Therapeutics, Inc. и ее дочерних компаний, включая, помимо прочего, Scilex, в соответствии с положениями о безопасной гавани Раздела 21E Закона о частных ценных бумагах. Закона о реформе 1995 года и подвержены рискам и неопределенностям, которые могут привести к тому, что фактические результаты будут существенно отличаться от запланированных. Прогнозные заявления включают заявления о предлагаемом объединении бизнеса между Scilex и VCKA, включая сроки такого объединения бизнеса, потенциальный листинг обыкновенных акций Объединенной компании на Nasdaq или другой крупной фондовой бирже и ожидаемый биржевой код для таких акций, ожидание того, что VCKA подаст регистрационное заявление по форме S-4 в SEC, которое будет включать доверенное заявление/проспект эмиссии, предполагаемые или ожидаемые будущие результаты и выгоды Объединенной компании после предлагаемого объединения бизнеса, включая вероятность и способность сторон успешно завершить предлагаемое объединение бизнеса, будущие возможности для Объединенной компании, сроки завершения предлагаемого объединения бизнеса, предлагаемые бизнес-стратегии Scilex и Объединенной компании, ожидаемые денежные ресурсы Объединенной компании и ожидаемое их использование; Scilex ожидает, что SP-102 (SEMDEXA™) станет первой одобренной FDA неопиоидной эпидуральной инъекцией для лечения ишиаса; Намерение Scilex использовать результаты ключевого исследования Фазы 3 для обсуждения с FDA заявки на получение лицензии и статус прорыва для ишиаса, а также для поддержки заявки на новое лекарство, а также сроков предполагаемой подачи NDA для SP-102; Текущие и потенциальные продукты-кандидаты Scilex и Объединенной компании, запланированные клинические испытания и доклинические мероприятия, а также потенциальные одобрения продуктов, а также возможность принятия рынком любых одобренных продуктов и соответствующие рыночные возможности; заявления относительно SP-102 (SEMDEXA™), если они одобрены FDA; планы развития и коммерциализации Scilex; а также продукты, технологии и перспективы Sorrento и продукты, технологии и перспективы Scilex, включая возможность того, что продукты-кандидаты Scilex станут лучшими в своем классе или первыми в своем классе методами лечения. Риски и неопределенности, которые могут привести к тому, что фактические результаты Sorrento и Scilex будут существенно и неблагоприятно отличаться от результатов, выраженных в наших прогнозных заявлениях, включают, помимо прочего: неспособность сторон завершить предлагаемую сделку по объединению бизнеса по любой причине или возникновение любого события, изменения или других обстоятельств, которые могут привести к прекращению действия ДСС, включая любое невыполнение применимых условий закрытия; изменения в структуре, сроках и завершении предполагаемой сделки между VCKA и Scilex; способность VCKA продолжать листинг на рынке капитала Nasdaq до закрытия предполагаемой сделки; способность Объединенной компании разместить свои ценные бумаги на Nasdaq или другой крупной фондовой бирже после закрытия предполагаемой сделки; способность сторон получить выгоды от предполагаемой сделки, включая будущие финансовые и операционные результаты Объединенной компании; способность сторон реализовать ожидаемый синергетический эффект от предполагаемой сделки; риски, связанные с исходом любого судебного разбирательства, которое может быть возбуждено против сторон после объявления о предлагаемом объединении бизнеса; общие экономические, политические и деловые условия; риски, связанные с продолжающимся COVID-19пандемия; риск того, что потенциальные продукты-кандидаты, которые разрабатывает Scilex, могут не пройти клиническую разработку или получить необходимые разрешения регулирующих органов в ожидаемые сроки или вообще не получить; риски, связанные с неопределенностью в отношении пути регулирования продуктов-кандидатов Scilex; риск того, что Scilex не сможет успешно продвигать на рынке или добиться признания на рынке своих продуктов-кандидатов; риск того, что продукты-кандидаты Scilex могут оказаться бесполезными для пациентов или быть неуспешно коммерциализированными; риск того, что Scilex переоценил размер целевой популяции пациентов, их готовность опробовать новые методы лечения и готовность врачей назначать эти методы лечения; риски того, что предыдущие результаты клинических испытаний SP-102 (SEMDEXA™) не могут быть воспроизведены; регуляторные риски и риски интеллектуальной собственности; риск того, что какие-либо необходимые разрешения регулирующих органов для завершения сделки не будут получены, будут задержаны или будут зависеть от непредвиденных условий, которые могут неблагоприятно повлиять на Объединенную компанию или ожидаемые выгоды от предлагаемой сделки, или что одобрение акционеров VCKA не будет получено; риск неполучения ожидаемых выгод от предполагаемой сделки; сумма запросов на выкуп, сделанных акционерами VCKA, и другие риски и неопределенности, указанные время от времени, и другие риски, указанные в документах Sorrento и VCKA, поданных в Комиссию по ценным бумагам и биржам.
Риски и неопределенности, которые могут привести к тому, что фактические результаты Sorrento и Scilex будут существенно и неблагоприятно отличаться от результатов, выраженных в наших прогнозных заявлениях, включают, помимо прочего: неспособность сторон завершить предлагаемую сделку по объединению бизнеса по любой причине или возникновение любого события, изменения или других обстоятельств, которые могут привести к прекращению действия ДСС, включая любое невыполнение применимых условий закрытия; изменения в структуре, сроках и завершении предполагаемой сделки между VCKA и Scilex; способность VCKA продолжать листинг на рынке капитала Nasdaq до закрытия предполагаемой сделки; способность Объединенной компании разместить свои ценные бумаги на Nasdaq или другой крупной фондовой бирже после закрытия предполагаемой сделки; способность сторон получить выгоды от предполагаемой сделки, включая будущие финансовые и операционные результаты Объединенной компании; способность сторон реализовать ожидаемый синергетический эффект от предполагаемой сделки; риски, связанные с исходом любого судебного разбирательства, которое может быть возбуждено против сторон после объявления о предлагаемом объединении бизнеса; общие экономические, политические и деловые условия; риски, связанные с продолжающимся COVID-19пандемия; риск того, что потенциальные продукты-кандидаты, которые разрабатывает Scilex, могут не пройти клиническую разработку или получить необходимые разрешения регулирующих органов в ожидаемые сроки или вообще не получить; риски, связанные с неопределенностью в отношении пути регулирования продуктов-кандидатов Scilex; риск того, что Scilex не сможет успешно продвигать на рынке или добиться признания на рынке своих продуктов-кандидатов; риск того, что продукты-кандидаты Scilex могут оказаться бесполезными для пациентов или быть неуспешно коммерциализированными; риск того, что Scilex переоценил размер целевой популяции пациентов, их готовность опробовать новые методы лечения и готовность врачей назначать эти методы лечения; риски того, что предыдущие результаты клинических испытаний SP-102 (SEMDEXA™) не могут быть воспроизведены; регуляторные риски и риски интеллектуальной собственности; риск того, что какие-либо необходимые разрешения регулирующих органов для завершения сделки не будут получены, будут задержаны или будут зависеть от непредвиденных условий, которые могут неблагоприятно повлиять на Объединенную компанию или ожидаемые выгоды от предлагаемой сделки, или что одобрение акционеров VCKA не будет получено; риск неполучения ожидаемых выгод от предполагаемой сделки; сумма запросов на выкуп, сделанных акционерами VCKA, и другие риски и неопределенности, указанные время от времени, и другие риски, указанные в документах Sorrento и VCKA, поданных в Комиссию по ценным бумагам и биржам. Инвесторов предупреждают, что они не должны чрезмерно полагаться на эти прогнозные заявления, которые действительны только на дату настоящего выпуска, и мы не берем на себя никаких обязательств по обновлению каких-либо прогнозных заявлений в этом пресс-релизе, за исключением случаев, когда это требуется по закону.
Инвесторов предупреждают, что они не должны чрезмерно полагаться на эти прогнозные заявления, которые действительны только на дату настоящего выпуска, и мы не берем на себя никаких обязательств по обновлению каких-либо прогнозных заявлений в этом пресс-релизе, за исключением случаев, когда это требуется по закону.
Контакты:
Для Scilex Holding Company
Джайсим Шах
Главный исполнительный директор
Холдинговая компания «Силекс»
960 Сан-Антонио-роуд
Пало-Альто, Калифорния 94303
Офис: (650) 516-4310
Электронная почта: [email protected]
Веб-сайт: www.sorrentotherapys.com и www.scilexholding.com
Контактное лицо для инвесторов и СМИ:
Контактное лицо: Dorman Followwill
Электронная почта: [email protected]
Веб-сайт: www.sorrentotherapys.com
Sorrento® и логотип Sorrento являются зарегистрированными товарными знаками Sorrento Therapeutics, Inc. ISTIX™ является товарным знаком Sorrento Therapeutics, Inc.
ISTIX™ является товарным знаком Sorrento Therapeutics, Inc.
SEMDEXA™ (SP-102) является товарным знаком, принадлежащим Semnur Pharmaceuticals, Inc., дочерней компании Scilex Holding Company. Запланирована проверка фирменного наименования FDA.
ZTlido® является зарегистрированным товарным знаком, принадлежащим Scilex Pharmaceuticals Inc., дочерней компании Scilex Holding Company.
Все остальные товарные знаки являются собственностью соответствующих владельцев.
© 2022 Sorrento Therapeutics, Inc. Все права защищены.
Каталожные номера
(1) Deyo & Weinstein 2001
(2) Хадсон Т.Дж., Эдлунд М.Дж., Стеффик Д.Е., Трипати С.П., Салливан М.Д. Эпидемиология регулярного употребления опиоидов по рецепту: результаты общенационального опроса населения. J Pain Symptom Manage 2008; 36(3): 280-8
(3) Чапарро Л.Е., Фурлан А.Д., Дешпанде А., Майлис Ганьон А. , Атлас С., Терк Д.К. Опиоиды по сравнению с плацебо или другими методами лечения хронической боли в пояснице. Кокрановская база данных Syst Rev 2013 (8): CD004959
, Атлас С., Терк Д.К. Опиоиды по сравнению с плацебо или другими методами лечения хронической боли в пояснице. Кокрановская база данных Syst Rev 2013 (8): CD004959
(4) Чоу Р., Тернер Дж. А., Девайн Э. Б., Хансен Р. Н., Салливан С. Д., Блазина И. и др. Эффективность и риски долгосрочной опиоидной терапии хронической боли: систематический обзор для семинара Национального института здравоохранения по пути профилактики. Ann Intern Med 2015; 162 (4): 276–86
(5) Годовой отчет об эпиднадзоре за рисками и исходами, связанными с наркотиками, США, 2019 г.. Центры по контролю и профилактике заболеваний
(6) https://www.cdc.gov/opioids/basics/epidemic.html
(7) Новости США Стивена Росса Джонсона: данные CDC о смертности от передозировки наркотиков впервые превысили 100 тысяч, 17 ноября 2021 г.
(8) Группа ресурсов для принятия решений. Хроническая боль: картина болезни и прогноз. 2016; 76 и 80
(9) Группа ресурсов для принятия решений. Хроническая боль: картина болезни и прогноз. 2016; 40
2016; 40
(10) Группа ресурсов для принятия решений. Хроническая боль: картина болезни и прогноз. 2016; 62
(11) Группа ресурсов для принятия решений. Хроническая боль: картина болезни и прогноз. 2016; 62
(12) Группа ресурсов для принятия решений. Хроническая боль: картина болезни и прогноз. 2016; 8
(13) МОМ: более 100 миллионов человек страдают от хронической боли в США, Эмили П. Уокер, вашингтонский корреспондент, MedPage Today, 30 июня 2011 г.,
.
(14) Внутренний отчет Syneos SP-102 по ишиасу, март 2021 г.
(15) Yoshina et al., 2019 и Ostelo, de Vet. Клинически важные исходы при болях в пояснице. Лучшая практика и исследования клинической ревматологии. Том 19, выпуск 4, август 2005 г., страницы 593-607.
Департамент доходов штата Орегон : Формы и публикации : Библиотека форм и публикаций : Штат Орегон
Формы и публикации
Найдите формы и публикации, необходимые для ведения бизнеса с Департаментом штата Орегон доходов здесь.
Примечание: Важно загрузить и сохранить форму на свой компьютер, а затем открыть ее в Adobe Reader, заполнить и распечатать. Мы не рекомендуем использовать веб-браузер для заполнения формы, так как могут возникнуть проблемы.
Навигация
- Текущие формы и публикации
- Поиск по всем формам
- Получить или найти формы за предыдущие годы
- Найти федеральные формы
- Заказать бумажные формы
Текущие формы и публикации
Просмотреть все формы и публикации текущего года по популярности или области программы. Выберите заголовок, чтобы просмотреть соответствующие формы, а затем используйте функцию поиска, чтобы найти форму или публикацию по имени, номеру формы, году или типу.
Популярные формы
Апелляционная комиссия по налогу на имущество (BOPTA)
Сигареты и табак
Комбинированный фонд заработной платы
Корпорация
Налог на корпоративную деятельность
Программы отсрочки
Электронные услуги
Зона предприятия
Освобождение для кухонных комбайнов
Промышленная собственность
Местный бюджет
Марихуана
Бюллетени доходов штата Орегон (ORB)
Другие счета агентства
Избирательный налог на транзитные предприятия
Удержание заработной платы и транзит
Личный доход
Нефть
Налог на имущество
Псилоцибин
Древесина
Транзитная самозанятость
Утилита
Поиск по всем формам
Используйте функции поиска и фильтрации, чтобы найти форму или публикацию по имени, номеру формы, году, категории или программе.

 Напротив, инъекционные стероиды, не зарегистрированные по прямому назначению, обычно обеспечивают облегчение боли на период от менее недели до одного месяца, после чего может потребоваться повторная инъекция.
Напротив, инъекционные стероиды, не зарегистрированные по прямому назначению, обычно обеспечивают облегчение боли на период от менее недели до одного месяца, после чего может потребоваться повторная инъекция.