7 § 8 Химия Габриелян 11 класс Чем отличается газообразное состояние вещества от твёрдого и жидкого? – Рамблер/класс
7 § 8 Химия Габриелян 11 класс Чем отличается газообразное состояние вещества от твёрдого и жидкого? – Рамблер/классИнтересные вопросы
Школа
Подскажите, как бороться с грубым отношением одноклассников к моему ребенку?
Новости
Поделитесь, сколько вы потратили на подготовку ребенка к учебному году?
Школа
Объясните, это правда, что родители теперь будут информироваться о снижении успеваемости в школе?
Школа
Когда в 2018 году намечено проведение основного периода ЕГЭ?
Новости
Будет ли как-то улучшаться система проверки и организации итоговых сочинений?
Вузы
Подскажите, почему закрыли прием в Московский институт телевидения и радиовещания “Останкино”?
Чем отличается газообразное состояние вещества от
твёрдого и жидкого?
ответы
Твердое состояние характеризуется способностью со-
хранять объём и форму. Атомы твёрдого тела совершают
Атомы твёрдого тела совершают
лишь небольшие колебания вокруг состояния равновесия.
Присутствует как дальний, так и ближний порядок.
Жидкое состояние — состояние вещества, при котором
оно обладает малой сжимаемостью, то есть хорошо сохраняет
объём, однако не способно сохранять форму. Жидкость легко
принимает форму сосуда, в который она помещена. Атомы
или молекулы жидкости совершают колебания вблизи состоя-
ния равновесия, запертые другими атомами, и часто переска-
кивают на другие свободные места. Присутствует только
ближний порядок.
Газообразное состояние характеризуется хорошей сжи-
маемостью, отсутствием способности сохранять как объём,
так и форму. Газ стремится занять весь объём, ему предостав-
ленный. Атомы или молекулы газа ведут себя относительно
свободно, расстояния между ними гораздо больше их разме-
ваш ответ
Можно ввести 4000 cимволов
отправить
дежурный
Нажимая кнопку «отправить», вы принимаете условия пользовательского соглашения
похожие темы
Юмор
Олимпиады
ЕГЭ
10 класс
похожие вопросы 3
Приготовление раствора сахара и расчёт его массовой доли в растворе. Химия. 8 класс. Габриелян. ГДЗ. Хим. практикум № 1. Практ. работа № 5.
Химия. 8 класс. Габриелян. ГДЗ. Хим. практикум № 1. Практ. работа № 5.
Попробуйте провести следующий опыт. Приготовление раствора
сахара и расчёт его массовой доли в растворе.
Отмерьте мерным (Подробнее…)
ГДЗШкола8 классХимияГабриелян О.С.
Здравствуйте.
(Подробнее…)
Химия
Какой был проходной балл в вузы в 2017 году?
Какой был средний балл ЕГЭ поступивших в российские вузы на бюджет в этом году? (Подробнее…)
Поступление11 классЕГЭНовости
Чем отличается газообразное состояние от жидкого и твердого?
Прочее › Чем отличается › Чем отличается газообразное состояние вещества от твердого и жидкого?
Чем отличается газообразное состояние вещества от твёрдого и жидкого? Для жидкого и твердого состояний характерна определенная упорядоченность частиц, для газа свойственно их независимое друг от друга расположение и отсутствие дальнего или ближнего порядка.
- В чем главное отличие газообразного вещества от жидкого и твердого?
- Чем отличается твердое состояние от жидкого?
- Чем отличается строение газообразного вещества от жидкого?
- Чем отличается твердое состояние вещества от газообразного?
- Чем отличаются жидкости и газы?
- Что происходит при переходе вещества из жидкого состояния в газообразное?
- Что происходит при переходе из жидкого состояния в твердое?
- Какая основная характерная особенность отличает твердое состояние вещества от жидкого и газообразного?
- Когда вода переходит в твердое состояние?
- Что относится к жидким веществам?
- В чем заключается особенности жидкого состояния вещества?
- Как называют тепловой процесс перехода вещества из газообразного состояния в жидкое?
- Что характеризует твердое состояние вещества?
- Что происходит при переходе вещества из жидкого состояния в твердое?
- Какое вещество переходит из твердого в газообразное минуя жидкое?
- Как называется явление перехода вещества из твердого агрегатного состояния в газообразное минуя жидкое?
В чем главное отличие газообразного вещества от жидкого и твердого?
Подобно жидкостям, газы обладают текучестью и сопротивляются деформации. В отличие от жидкостей, газы не имеют фиксированного объёма, а стремятся заполнить весь доступный объём (например, сосуда). В планетарном масштабе газ в атмосфере удерживается гравитацией и не образует свободной поверхности.
В отличие от жидкостей, газы не имеют фиксированного объёма, а стремятся заполнить весь доступный объём (например, сосуда). В планетарном масштабе газ в атмосфере удерживается гравитацией и не образует свободной поверхности.
Чем отличается твердое состояние от жидкого?
Расстояние между молекулами в жидком состоянии чуть больше, чем в твердом, но все равно невелико. При этом частицы не собраны в кристаллическую решетку, а расположены хаотично. Молекулы почти не двигаются, но при нагревании жидкости делают это более охотно.
Чем отличается строение газообразного вещества от жидкого?
У газообразного вещества промежутки между молекулами в несколько раз больше, чем у жидкого. И газообразное и жидкое — все это разные агрегатные состояние одного вещества.
Чем отличается твердое состояние вещества от газообразного?
Расстояние между молекулами, образующими газ, наибольшее по сравнению с твердыми и жидкими телами. В газе частицы перемещаются максимально хаотично, взаимодействуя незначительно.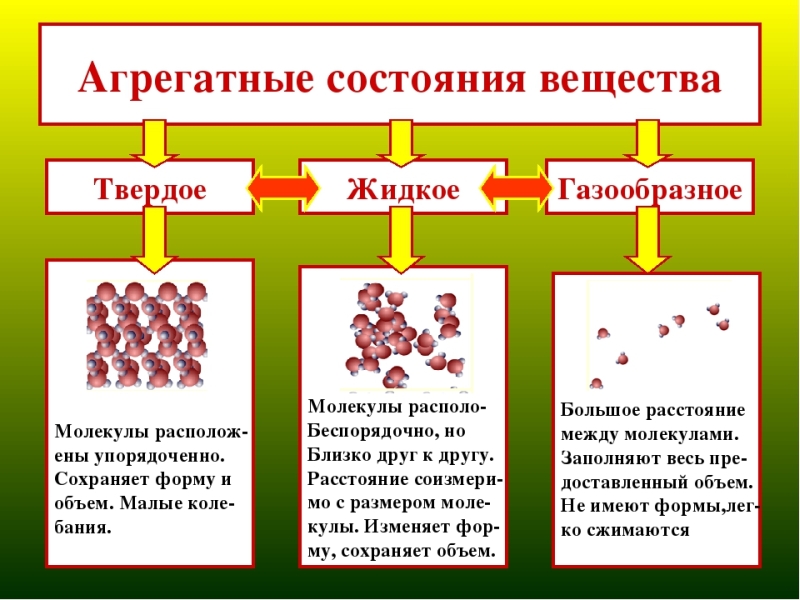 Такое расположение частиц обеспечивает маленькую плотность газов и отсутствие у них собственной формы (газы обладают большой сжимаемостью).
Такое расположение частиц обеспечивает маленькую плотность газов и отсутствие у них собственной формы (газы обладают большой сжимаемостью).
Чем отличаются жидкости и газы?
Жидкость — это вещество, которое свободно течет, имеет определенный объем, но не имеет постоянной формы. Газ относится к состоянию вещества, которое не имеет какой-либо формы, но полностью соответствует форме контейнера, в которую оно помещается. Твердые тела имеют фиксированную форму и объем.
Что происходит при переходе вещества из жидкого состояния в газообразное?
Переход вещества из жидкого состояния в газообразное называется парообразованием. Переход вещества из газообразного состояния в жидкое называется конденсацией.
Что происходит при переходе из жидкого состояния в твердое?
В процессе перехода вещества из жидкого состояния в твердое происходит построение кристаллической решетки, а значит, существенно увеличивается упорядоченность в расположении молекул вещества.
Какая основная характерная особенность отличает твердое состояние вещества от жидкого и газообразного?
Твёрдое тело Твёрдое те́ло — одно из четырёх основных агрегатных состояний вещества, отличающееся от других агрегатных состояний (жидкости, газов, плазмы) стабильностью формы и характером теплового движения атомов, совершающих малые колебания около положений равновесия.
Когда вода переходит в твердое состояние?
Переход воды из жидкого в твердое состояние происходит при 0 градусов (по Цельсию).
Что относится к жидким веществам?
Жидкие вещества: вода, спирт, молоко, ртуть, уксус. Эти вещества текучи и принимают форму сосуда, в котором находятся. Газообразные вещества: углекислый газ, природный газ, кислород.
В чем заключается особенности жидкого состояния вещества?
Они имеют одинаковые свойства по всем направлениям (изотропны), ближний порядок в расположении частиц, у них нет температуры плавления (при нагреве вещество постепенно размягчается и переходит в жидкое состояние).
Как называют тепловой процесс перехода вещества из газообразного состояния в жидкое?
Переход из жидкого в газообразное состояние называют испарением, а противоположный ему переход из газообразного состояния в жидкое — конденсацией.
Что характеризует твердое состояние вещества?
Вещество в твердом состоянии сохраняет форму и объем. Это объясняется тем, что частицы вещества (атомы или молекулы) сохраняют свое положение относительно друг друга и соединены друг с другом межатомными или межмолекулярными связями. Частицы совершают лишь небольшие колебательные тепловые движения.
Это объясняется тем, что частицы вещества (атомы или молекулы) сохраняют свое положение относительно друг друга и соединены друг с другом межатомными или межмолекулярными связями. Частицы совершают лишь небольшие колебательные тепловые движения.
Что происходит при переходе вещества из жидкого состояния в твердое?
В процессе перехода вещества из жидкого состояния в твердое происходит построение кристаллической решетки, а значит, существенно увеличивается упорядоченность в расположении молекул вещества.
Какое вещество переходит из твердого в газообразное минуя жидкое?
Переход из твердого агрегатного состояния в газообразное, минуя жидкое называется «сублимация». Подобное явления можно наблюдать при испарении углекислого газ, твердого йода и др.
Как называется явление перехода вещества из твердого агрегатного состояния в газообразное минуя жидкое?
Переход из твёрдого состояния в газообразное, минуя жидкое, называют сублимацией или возгонкой.
3.
 3: Классификация вещества по состоянию: твердое, жидкое и газообразное
3: Классификация вещества по состоянию: твердое, жидкое и газообразное- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 129654
Цели обучения
- Дать описание твердой, жидкой и газообразной фаз. 9\text{o} \text{C}\), вода – это газ (пар). Состояние, в котором находится вода, зависит от температуры. Каждое состояние имеет свой уникальный набор физических свойств. Материя обычно существует в одном из трех состояний: твердое , жидкое или газообразное . Рисунок \(\PageIndex{1}\): Материя обычно классифицируется по трем классическим состояниям, иногда к четвертому состоянию добавляется плазма.
 Слева направо: кварц (твердое), вода (жидкое), диоксид азота (газ). Состояние, которое проявляет данное вещество, также является физическим свойством. Некоторые вещества существуют в виде газов при комнатной температуре (кислород и углекислый газ), а другие, например вода и металлическая ртуть, существуют в виде жидкостей. Большинство металлов существует в твердом состоянии при комнатной температуре. Все вещества могут находиться в любом из этих трех состояний. На рисунке \(\PageIndex{2}\) показаны различия между твердыми телами, жидкостями и газами на молекулярном уровне. Твердое тело имеет определенный объем и форму, жидкость имеет определенный объем, но не имеет определенной формы, а газ не имеет ни определенного объема, ни определенной формы. Рисунок \(\PageIndex{2}\): Представление твердого, жидкого и газообразного состояний. (а) Твердое тело O 2 имеет фиксированный объем и форму, а молекулы плотно упакованы. b) жидкость O 2 соответствует форме контейнера, но имеет фиксированный объем; он содержит относительно плотно упакованные молекулы.
Слева направо: кварц (твердое), вода (жидкое), диоксид азота (газ). Состояние, которое проявляет данное вещество, также является физическим свойством. Некоторые вещества существуют в виде газов при комнатной температуре (кислород и углекислый газ), а другие, например вода и металлическая ртуть, существуют в виде жидкостей. Большинство металлов существует в твердом состоянии при комнатной температуре. Все вещества могут находиться в любом из этих трех состояний. На рисунке \(\PageIndex{2}\) показаны различия между твердыми телами, жидкостями и газами на молекулярном уровне. Твердое тело имеет определенный объем и форму, жидкость имеет определенный объем, но не имеет определенной формы, а газ не имеет ни определенного объема, ни определенной формы. Рисунок \(\PageIndex{2}\): Представление твердого, жидкого и газообразного состояний. (а) Твердое тело O 2 имеет фиксированный объем и форму, а молекулы плотно упакованы. b) жидкость O 2 соответствует форме контейнера, но имеет фиксированный объем; он содержит относительно плотно упакованные молекулы.
Плазма: четвертое состояние вещества
С технической точки зрения существует четвертое состояние материи, называемое плазмой, но оно не встречается в природе на Земле, поэтому мы не будем его здесь изучать.
Плазменный шар, работающий в затемненной комнате. (CC BY-SA 3.0; Шоколадный дуб).
Твердые тела
В твердом состоянии отдельные частицы вещества находятся в фиксированном положении по отношению друг к другу, поскольку тепловой энергии недостаточно для преодоления межмолекулярных взаимодействий между частицами. В результате твердые тела имеют определенную форму и объем. Большинство твердых веществ твердые, но некоторые (например, воски) относительно мягкие. Многие твердые тела, состоящие из ионов, также могут быть довольно хрупкими. 9\text{o} \text{C}\), и при правильном давлении мы заметили бы, что все жидкие частицы перешли бы в твердое состояние.
Ртуть может затвердеть, если ее температура доводится до точки замерзания. Однако при возвращении в условия комнатной температуры ртуть недолго существует в твердом состоянии и возвращается в свою более обычную жидкую форму.
Частицы, из которых состоят твердые тела, обычно располагаются в регулярном трехмерном массиве чередующихся положительных и отрицательных ионов, называемом кристалл . Эффект такого регулярного расположения частиц иногда виден макроскопически, как показано на рисунке \(\PageIndex{3}\). Некоторые твердые тела, особенно состоящие из крупных молекул, не могут легко организовать свои частицы в такие правильные кристаллы и существуют в виде аморфных (буквально «бесформенных») твердых тел. Стекло является одним из примеров аморфного твердого тела.
Рисунок \(\PageIndex{3}\): (слева) Периодическая структура кристаллической решетки кварца \(SiO_2\) в двух измерениях. (справа) Случайная сетчатая структура стеклообразного \(SiO_2\) в двух измерениях.
Жидкости
Если частицы вещества обладают достаточной энергией для частичного преодоления межмолекулярных взаимодействий, то частицы могут двигаться относительно друг друга, оставаясь при этом в контакте. Это описывает жидкое состояние. В жидкости частицы все еще находятся в тесном контакте, поэтому жидкости имеют определенный объем. Однако, поскольку частицы могут довольно свободно перемещаться относительно друг друга, жидкость не имеет определенной формы и принимает форму, диктуемую ее сосудом.
Жидкости имеют следующие характеристики:
- Не имеет определенной формы (принимает форму контейнера).
- Имеет определенный объем.
- Частицы могут свободно перемещаться друг над другом, но по-прежнему притягиваются друг к другу.

Знакомая жидкость — металлическая ртуть. Меркурий – аномалия. Это единственный известный нам металл, который находится в жидком состоянии при комнатной температуре. Ртуть также обладает способностью прилипать к самой себе (поверхностное натяжение) — свойство, присущее всем жидкостям. Ртуть имеет относительно высокое поверхностное натяжение, что делает ее уникальной. Здесь вы видите ртуть в ее обычной жидкой форме. 9\text{o} \text{C}\) при правильном давлении мы бы заметили, что все частицы в жидком состоянии переходят в газообразное состояние.
Газы
Если частицы вещества обладают достаточной энергией для полного преодоления межмолекулярных взаимодействий, то частицы могут отделяться друг от друга и беспорядочно перемещаться в пространстве. Это описывает состояние газа, которое мы рассмотрим более подробно в другом месте. Как и жидкости, газы не имеют определенной формы, но в отличие от твердых тел и жидкостей у газов нет и определенного объема. Переход из твердого состояния в жидкое обычно не приводит к существенному изменению объема вещества.

- Не имеет определенной формы (принимает форму контейнера)
- Нет определенного объема
- Частицы движутся случайным образом практически без притяжения друг к другу
- Высокая сжимаемость
Таблица \(\PageIndex{1}\): Характеристики трех состояний вещества Характеристики Твердые вещества Жидкости Газы Форма определенный неопределенный неопределенный объем определенный определенный неопределенный относительная сила межмолекулярного взаимодействия сильный умеренный слабый относительное положение частиц в контакте и закреплен на месте в контакте, но не зафиксировано не в контакте, случайные положения Пример \(\PageIndex{1}\)
Какое состояние или состояния материи описывает каждое утверждение?
- Это состояние имеет определенный объем, но не определенную форму.

- В этом состоянии нет определенного объема.
- Это состояние позволяет отдельным частицам двигаться, оставаясь при этом в контакте.
Раствор
- Это утверждение описывает жидкое состояние.
- Этот оператор описывает состояние газа.
- Это утверждение описывает жидкое состояние.
Упражнение \(\PageIndex{1}\)
Какое состояние или состояния материи описывает каждое утверждение?
- В этом состоянии отдельные частицы находятся в фиксированном положении по отношению друг к другу.
- В этом состоянии отдельные частицы находятся далеко друг от друга в пространстве.
- Это состояние имеет определенную форму.
- Ответ a:
- твердый
- Ответ б:
- газ
- Ответ c:
- твердый
Резюме
- Существует три состояния вещества — твердое, жидкое и газообразное.

- Твердые тела имеют определенную форму и объем.
- Жидкости имеют определенный объем, но принимают форму сосуда.
- Газы не имеют определенной формы или объема.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу TOC
- № на стр.
- Включено
- да
- Теги

7.2: Твердые вещества, жидкости и газы
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 59257
- Дать описание твердой и жидкой фаз.
- Это состояние имеет определенный объем.

- Это состояние не имеет определенной формы.
- Это состояние позволяет отдельным частицам двигаться, оставаясь при этом в контакте.
- Это утверждение описывает жидкое или твердое состояние.
- Это выражение описывает жидкое или газообразное состояние.
- Это утверждение описывает жидкое состояние.
- В этом состоянии отдельные частицы находятся в фиксированном положении по отношению друг к другу.
- В этом состоянии отдельные частицы находятся далеко друг от друга в пространстве.
- Это состояние имеет определенную форму.
- Ответить
а. твердый
б. газ
с. твердый
- Твердые и жидкие фазы — это фазы, обладающие своими уникальными свойствами.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу TOC
- № на стр.

Цели обучения
Твердые и жидкие вещества вместе называются конденсированными фазами , поскольку их частицы находятся в виртуальном контакте. Однако у двух штатов мало общего.
Твердые тела
В твердом состоянии отдельные частицы вещества находятся в фиксированном положении по отношению друг к другу, поскольку тепловой энергии недостаточно для преодоления межмолекулярных взаимодействий между частицами. В результате твердые тела имеют определенную форму и объем. Большинство твердых веществ твердые, но некоторые (например, воски) относительно мягкие. Многие твердые тела, состоящие из ионов, также могут быть довольно хрупкими.
Большинство твердых веществ твердые, но некоторые (например, воски) относительно мягкие. Многие твердые тела, состоящие из ионов, также могут быть довольно хрупкими.
Частицы, из которых состоят твердые тела, обычно располагаются в виде правильного трехмерного массива чередующихся положительных и отрицательных ионов, называемого кристаллом. Эффект такого регулярного расположения частиц иногда виден макроскопически, как показано на рисунке \(\PageIndex{1}\). Некоторые твердые тела, особенно состоящие из крупных молекул, не могут легко организовать свои частицы в такие правильные кристаллы и существуют в виде аморфных (буквально «бесформенных») твердых тел. Стекло является одним из примеров аморфного твердого тела.
Жидкости
Если частицы вещества обладают достаточной энергией для частичного преодоления межмолекулярных взаимодействий, то частицы могут двигаться относительно друг друга, оставаясь при этом в контакте. Это описывает жидкое состояние. В жидкости частицы все еще находятся в тесном контакте, поэтому жидкости имеют определенный объем. Однако, поскольку частицы могут довольно свободно перемещаться относительно друг друга, жидкость не имеет определенной формы и принимает форму, диктуемую ее сосудом.
Это описывает жидкое состояние. В жидкости частицы все еще находятся в тесном контакте, поэтому жидкости имеют определенный объем. Однако, поскольку частицы могут довольно свободно перемещаться относительно друг друга, жидкость не имеет определенной формы и принимает форму, диктуемую ее сосудом.
Газы
Если частицы вещества обладают достаточной энергией для полного преодоления межмолекулярных взаимодействий, то частицы могут отделяться друг от друга и беспорядочно перемещаться в пространстве. Как и жидкости, газы не имеют определенной формы, но в отличие от твердых тел и жидкостей у газов нет и определенного объема.
Рисунок \(\PageIndex{3}\): Представление твердого, жидкого и газообразного состояний. Твердое тело имеет определенный объем и форму, жидкость имеет определенный объем, но не имеет определенной формы, а газ не имеет ни определенного объема, ни определенной формы.
Переход из твердого состояния в жидкое обычно существенно не меняет объем вещества. Однако переход из жидкости в газ значительно увеличивает объем вещества в 1000 и более раз. На рисунке \(\PageIndex{3}\) показаны различия между твердыми телами, жидкостями и газами на молекулярном уровне, а в таблице \(\PageIndex{1}\) перечислены различные характеристики этих состояний.
| Характеристика | Твердый | Жидкость | Газ |
|---|---|---|---|
| форма | определенный | неопределенный | неопределенный |
| объем | определенный | определенный | неопределенный |
| относительная сила межмолекулярного взаимодействия | сильный | умеренный | слабый |
| относительное положение частиц | в контакте и закреплен на месте | в контакте, но не зафиксировано | не в контакте, случайные положения |
Пример \(\PageIndex{1}\)
Какое состояние или состояния материи описывает каждое утверждение?
Решение
Упражнение \(\PageIndex{1}\)
Какое состояние или состояния материи описывает каждое утверждение?
Взгляд поближе: вода, самая важная жидкость
Земля — единственное известное тело в нашей Солнечной системе, на поверхности которого свободно существует жидкая вода. Это хорошо, потому что жизнь на Земле была бы невозможна без присутствия жидкой воды.
Это хорошо, потому что жизнь на Земле была бы невозможна без присутствия жидкой воды.
Вода обладает рядом свойств, которые делают ее уникальным веществом среди других веществ. Это отличный растворитель; он растворяет многие другие вещества и позволяет этим веществам реагировать в растворе. На самом деле воду иногда называют универсальным растворителем из-за этой способности. Вода имеет необычно высокие температуры плавления и кипения (0°C и 100°C соответственно) для такой маленькой молекулы. Температуры кипения для молекул аналогичного размера, таких как метан (точка кипения = -162°C) и аммиак (точка кипения = -33°C), более чем на 100° ниже. Хотя молекулы воды являются жидкостью при нормальных температурах, они испытывают относительно сильное межмолекулярное взаимодействие, которое позволяет им сохранять жидкую фазу при более высоких температурах, чем ожидалось.
В отличие от большинства веществ, твердая форма воды менее плотна, чем жидкая, что позволяет льду плавать на поверхности воды. Наиболее энергетически выгодной конфигурацией молекул H 2 O является та, в которой каждая молекула связана водородными связями с четырьмя соседними молекулами. Благодаря тепловым движениям этот идеал никогда не достигается в жидкости, но когда вода замерзает и превращается в лед, молекулы располагаются именно в таком порядке в кристалле льда. Такое расположение требует, чтобы молекулы находились несколько дальше друг от друга, чем это было бы в противном случае; как следствие, лед, в котором водородные связи максимальны, имеет более открытую структуру и, следовательно, меньшую плотность, чем вода.
Наиболее энергетически выгодной конфигурацией молекул H 2 O является та, в которой каждая молекула связана водородными связями с четырьмя соседними молекулами. Благодаря тепловым движениям этот идеал никогда не достигается в жидкости, но когда вода замерзает и превращается в лед, молекулы располагаются именно в таком порядке в кристалле льда. Такое расположение требует, чтобы молекулы находились несколько дальше друг от друга, чем это было бы в противном случае; как следствие, лед, в котором водородные связи максимальны, имеет более открытую структуру и, следовательно, меньшую плотность, чем вода.
Вот трехмерные изображения типичной локальной структуры воды (слева) и льда (справа). Обратите внимание на большую открытость структуры льда, которая необходима для обеспечения наиболее сильной степени водородных связей в однородной протяженной кристаллической решетке. Структура жидкой воды очень похожа, но в жидкости водородные связи постоянно разрываются и образуются из-за быстрого движения молекул. Поскольку лед менее плотный, чем жидкая вода, реки, озера и океаны замерзают сверху вниз. Фактически лед образует защитный поверхностный слой, который изолирует остальную часть воды, позволяя рыбам и другим организмам выживать на нижних уровнях замерзшего озера или моря. Если бы лед был плотнее жидкости, лед, образовавшийся на поверхности в холодную погоду, тонул бы так же быстро, как образовался. Водоемы замерзнут снизу вверх, что будет смертельно для большинства водных существ. Расширение воды при замерзании также объясняет, почему автомобильные или лодочные двигатели необходимо защищать «антифризом» и почему незащищенные трубы в домах рвутся, если дать им замерзнуть.
Структура жидкой воды очень похожа, но в жидкости водородные связи постоянно разрываются и образуются из-за быстрого движения молекул. Поскольку лед менее плотный, чем жидкая вода, реки, озера и океаны замерзают сверху вниз. Фактически лед образует защитный поверхностный слой, который изолирует остальную часть воды, позволяя рыбам и другим организмам выживать на нижних уровнях замерзшего озера или моря. Если бы лед был плотнее жидкости, лед, образовавшийся на поверхности в холодную погоду, тонул бы так же быстро, как образовался. Водоемы замерзнут снизу вверх, что будет смертельно для большинства водных существ. Расширение воды при замерзании также объясняет, почему автомобильные или лодочные двигатели необходимо защищать «антифризом» и почему незащищенные трубы в домах рвутся, если дать им замерзнуть.
Вода также требует необычно большого количества энергии для изменения температуры. Если 100 Дж энергии изменит температуру 1 г Fe на 230°C, то такое же количество энергии изменит температуру 1 г H 2 O всего на 100°C. Таким образом, вода медленно меняет свою температуру по мере добавления или отвода тепла. Это оказывает серьезное влияние на погоду, поскольку штормовые системы, такие как ураганы, могут зависеть от количества тепла, которое может хранить океанская вода.
Таким образом, вода медленно меняет свою температуру по мере добавления или отвода тепла. Это оказывает серьезное влияние на погоду, поскольку штормовые системы, такие как ураганы, могут зависеть от количества тепла, которое может хранить океанская вода.
Влияние воды на окружающий мир зависит от этих свойств. Разве не удивительно, что такая маленькая молекула может иметь такое большое влияние?
Key Takeaway
7.2: Solids, Liquids, and Gases распространяется под лицензией CC BY-NC-SA 4.0, автором, ремиксом и/или куратором является LibreTexts.

 Слева направо: кварц (твердое), вода (жидкое), диоксид азота (газ). Состояние, которое проявляет данное вещество, также является физическим свойством. Некоторые вещества существуют в виде газов при комнатной температуре (кислород и углекислый газ), а другие, например вода и металлическая ртуть, существуют в виде жидкостей. Большинство металлов существует в твердом состоянии при комнатной температуре. Все вещества могут находиться в любом из этих трех состояний. На рисунке \(\PageIndex{2}\) показаны различия между твердыми телами, жидкостями и газами на молекулярном уровне. Твердое тело имеет определенный объем и форму, жидкость имеет определенный объем, но не имеет определенной формы, а газ не имеет ни определенного объема, ни определенной формы. Рисунок \(\PageIndex{2}\): Представление твердого, жидкого и газообразного состояний. (а) Твердое тело O 2 имеет фиксированный объем и форму, а молекулы плотно упакованы. b) жидкость O 2 соответствует форме контейнера, но имеет фиксированный объем; он содержит относительно плотно упакованные молекулы.
Слева направо: кварц (твердое), вода (жидкое), диоксид азота (газ). Состояние, которое проявляет данное вещество, также является физическим свойством. Некоторые вещества существуют в виде газов при комнатной температуре (кислород и углекислый газ), а другие, например вода и металлическая ртуть, существуют в виде жидкостей. Большинство металлов существует в твердом состоянии при комнатной температуре. Все вещества могут находиться в любом из этих трех состояний. На рисунке \(\PageIndex{2}\) показаны различия между твердыми телами, жидкостями и газами на молекулярном уровне. Твердое тело имеет определенный объем и форму, жидкость имеет определенный объем, но не имеет определенной формы, а газ не имеет ни определенного объема, ни определенной формы. Рисунок \(\PageIndex{2}\): Представление твердого, жидкого и газообразного состояний. (а) Твердое тело O 2 имеет фиксированный объем и форму, а молекулы плотно упакованы. b) жидкость O 2 соответствует форме контейнера, но имеет фиксированный объем; он содержит относительно плотно упакованные молекулы.








